艾诺韦林(Ainuovirine, ANV)是新一代非核苷类逆转录酶抑制剂(NNRTI),被国家科技部纳入国家十三五“重大新药创制”科技重大专项,于2021年6月获批上市,当年即被《中国艾滋病诊疗指南(2021版)》推荐,并成功纳入国家医保目录。
艾诺韦林3期临床试验数据 ACC007-301研究于2023年4月23日登上The Lancet Regional Health – Western Pacific 期刊,在线全文发表。

艾诺韦林对照依非韦伦联合拉米夫定/富马酸替诺福韦二吡呋酯治疗初治HIV-1阳性成人的有效性和安全性:
随机双盲48周3期临床试验,开放标签随访至96周
https://www.thelancet.com/journals/lanwpc/article/PIIS2666-6065(23)00087-1/fulltext
https://www.sciencedirect.com/science/article/pii/S2666606523000871
本研究是一项为期48周的多中心、随机、双盲双模拟、阳性平行对照、非劣性3期临床试验,对比艾诺韦林+3TC+TDF与EFV+3TC+TDF的联合用药方案的疗效和安全性,每日一次,双盲状态下治疗48周,揭盲后按受试者意愿选择治疗方案延长开放治疗至96周。在中国6个城市的7个临床中心进行,首都医科大学附属北京佑安医院、首都医科大学附属北京地坛医院、重庆市公共卫生医疗救治中心、广州医科大学附属市八医院、河南省传染病医院、江苏省传染病医院和长沙市第一医院。本文第一作者:粟斌、郜桂菊、王敏、鲁雁秋、李凌华、陈晨、陈媛媛;通讯作者:赵清霞、魏洪霞、蔡卫平、陈耀凯、张福杰、吴昊。
临床试验登记号:ChiCTR1800019041。
本期,我们特邀艾诺韦林3期临床试验的牵头人首都医科大学附属北京佑安医院的吴昊教授来解读这项研究,共同探讨中国艾滋病抗病毒治疗的优选方案。

本研究最终共纳入630名符合入组条件的HIV-1阳性初治成年感染者。
1、入组标准:确诊HIV-1阳性;未接受过抗HIV药物或治疗性疫苗的治疗;18~65 岁;HIV RNA≥1000 拷贝/mL等
2、排除标准:怀孕、哺乳、患有严重肝损伤、肾功能衰竭、严重免疫疾病、精神疾病或活动性肺结核合并感染等
3、主要终点:在第48周达到HIV RNA<50拷贝/mL的受试者比例,非劣效性界值设定为10%
4、次要疗效终点:
l HIV RNA的对数变化
l HIV RNA水平≤400拷贝/mL的受试者百分比
l 治疗48周和96周后CD4+T细胞计数的变化
l 治疗96周时HIV RNA水平<50拷贝/mL受试者的百分比
5、安全性终点:药物不良反应与实验室检查异常发生率
6、基线特征:
平均年龄为30.6±9.4岁,大多数参与者为男性(94.6%),80%以上汉族等
7、试验流程:
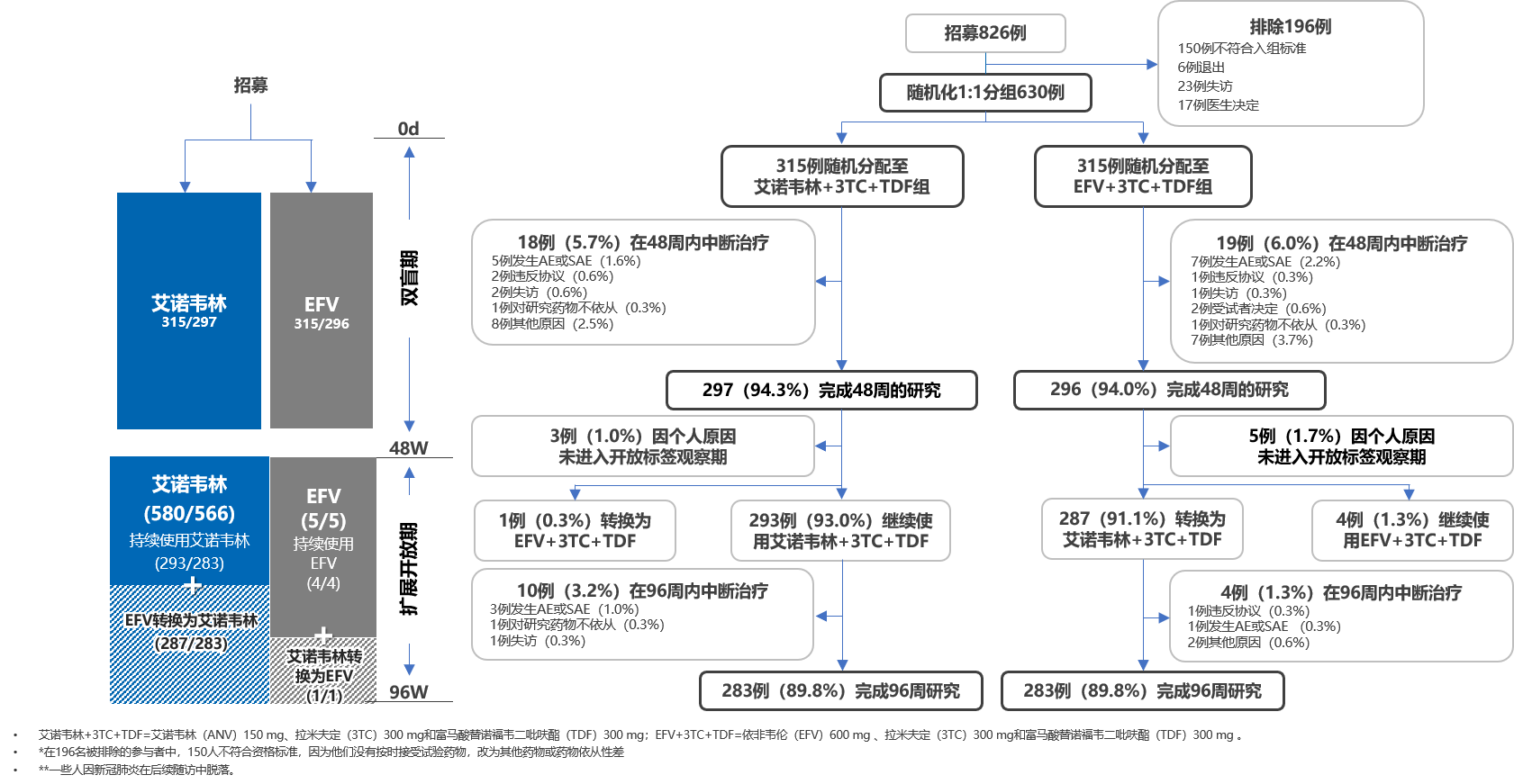
8、结果显示:
病毒学抑制
艾诺韦林组抗病毒疗效与EFV组相当,初始治疗48周可获得良好的病毒学抑制,扩展至96周病毒学抑制持续有效。在第48周,ANV组315名受试者中有274人(87.0%)和EFV组314名受试者中的288人(91.7%)达到HIV-1 RNA<50拷贝/mL,艾诺韦林方案相较EFV方案显示出非劣效性(差异:-4.7%,95%置信区间:-9.6%至0.1%)。治疗96周艾诺韦林持续治疗组和EFV经治转换为艾诺韦林组病毒持续抑制率均达到90%以上(组间无差异,p=0.189)。
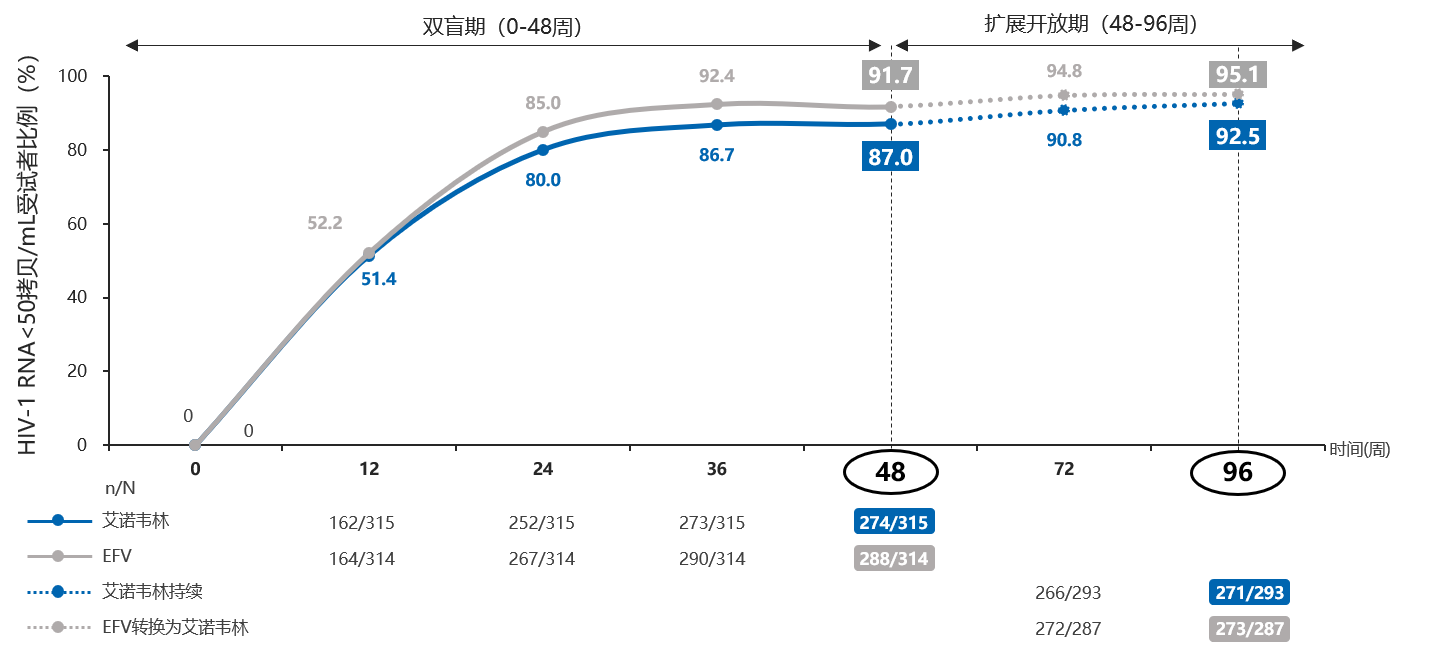
Log10 HIV-1 RNA 与基线相比的平均变化:第48周,艾诺韦林组变化为-2.90(95%可信区间:-2.91至-2.75),EFV组为-2.80(-2.89至-2.74)。
免疫重建
初始治疗48周,艾诺韦林组较EFV组可获得更好的免疫重建;扩展至96周,艾诺韦林持续治疗组免疫重建优于EFV转换为艾诺韦林组。
治疗48周艾诺韦林组CD4+T细胞计数的平均值增加高于对照组EFV组(134 /μL VS 122 /μL, p<0.05 );治疗96周艾诺韦林持续治疗组CD4+T细胞计数的平均值增加高于EFV转换为艾诺韦林组(181 /μL VS 169 /μL, p<0.05 )
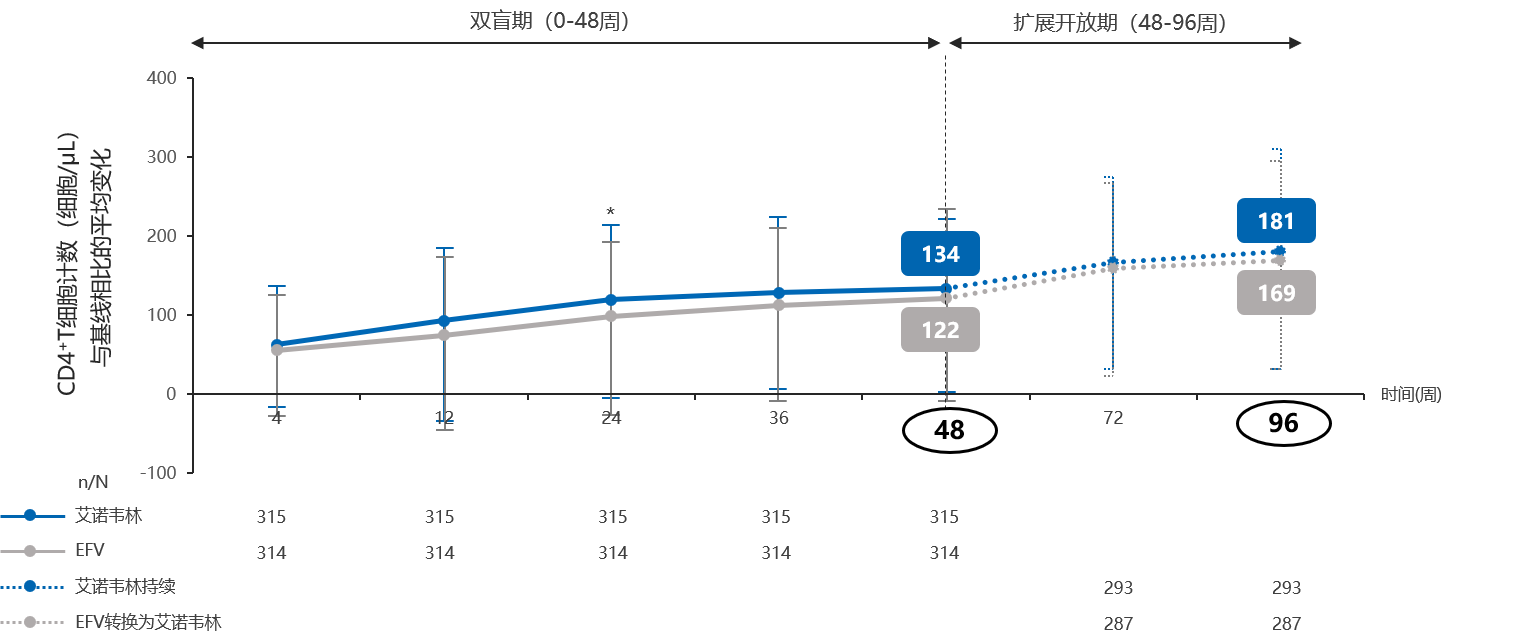
总体安全性
初始治疗48周ANV组315名受试者NNRTI治疗相关不良事件(TEAEs)的发生率为67.6%,显著低于EFV组314名受试者的91.4%(p <0.001)。EFV转换为艾诺韦林再治疗48周,不良事件发生率降低(91.4%降至64.1%)。
血脂友好
初始治疗48周,艾诺韦林组血脂异常发生率显著低于EFV组,对LDL-C、TG、TC具有优效性;EFV转换为艾诺韦林再治疗48周,血脂异常发生率降低,TG、TC改善。
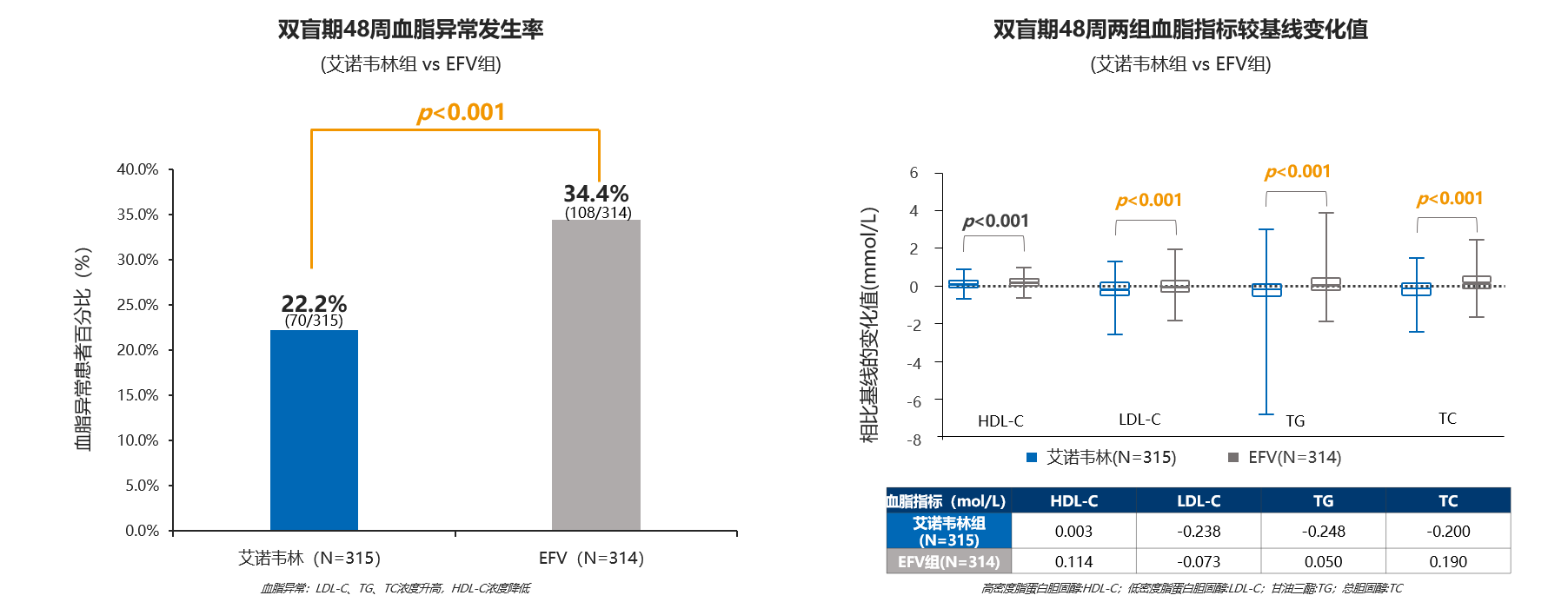
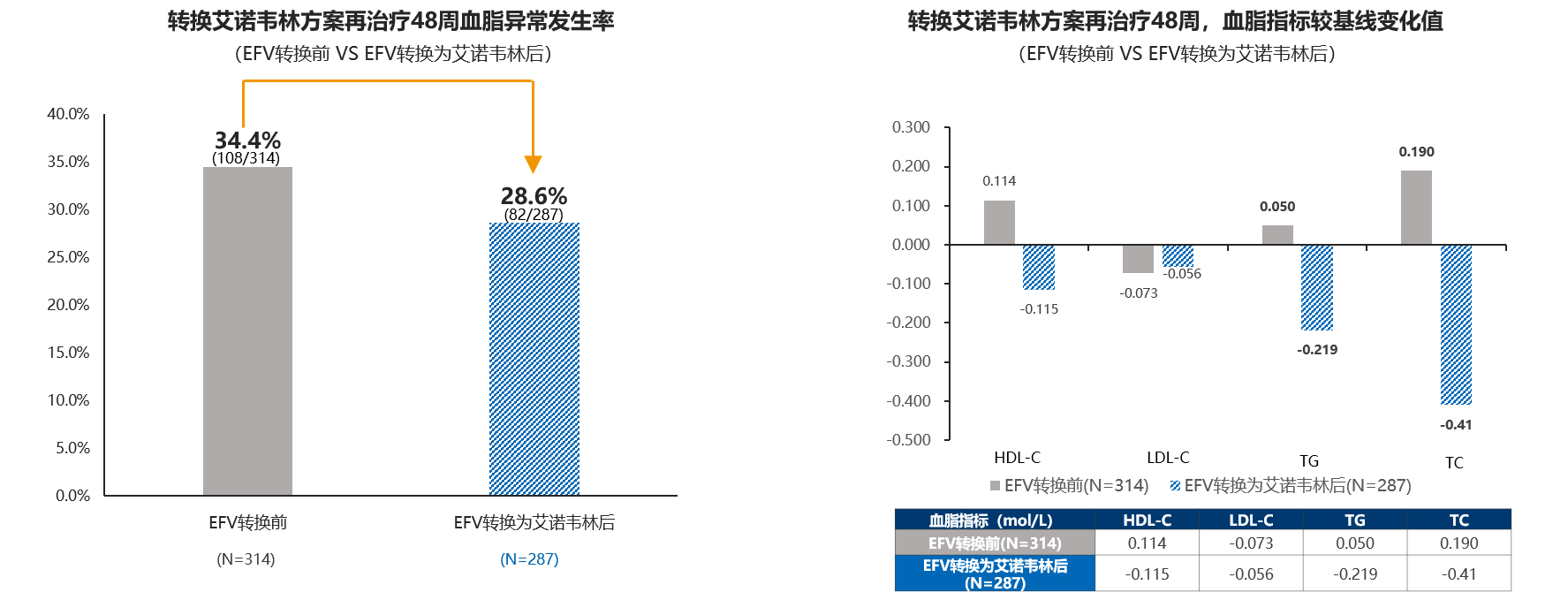
CNS改善
初始治疗48周,艾诺韦林组中枢神经系统不良反应发生率显著低于EFV组;EFV转换为艾诺韦林再治疗48周后,中枢神经系统不良反应发生率降低。
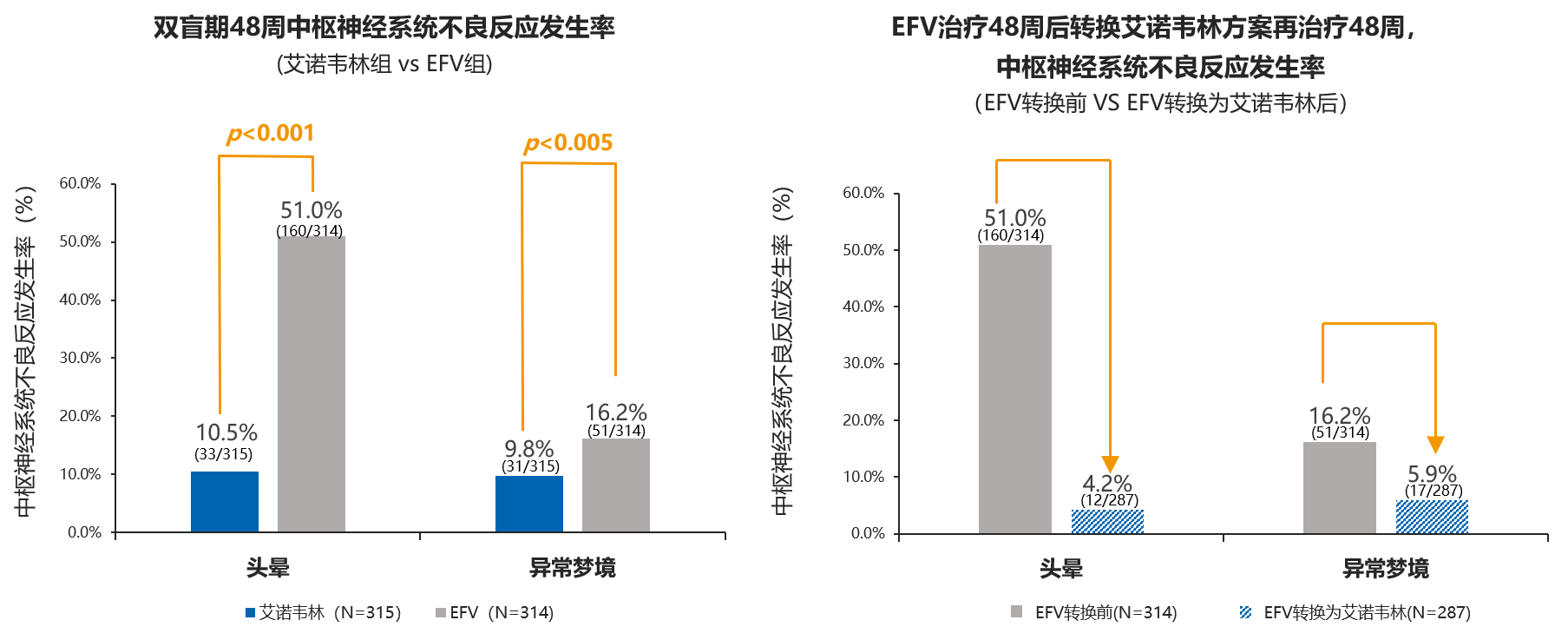
肝损发生率降低
初始治疗48周,艾诺韦林组对肝酶的影响显著低于EFV组,肝酶升高患者更少;EFV转换为艾诺韦林再治疗48周后,肝酶升高患者比例降低。
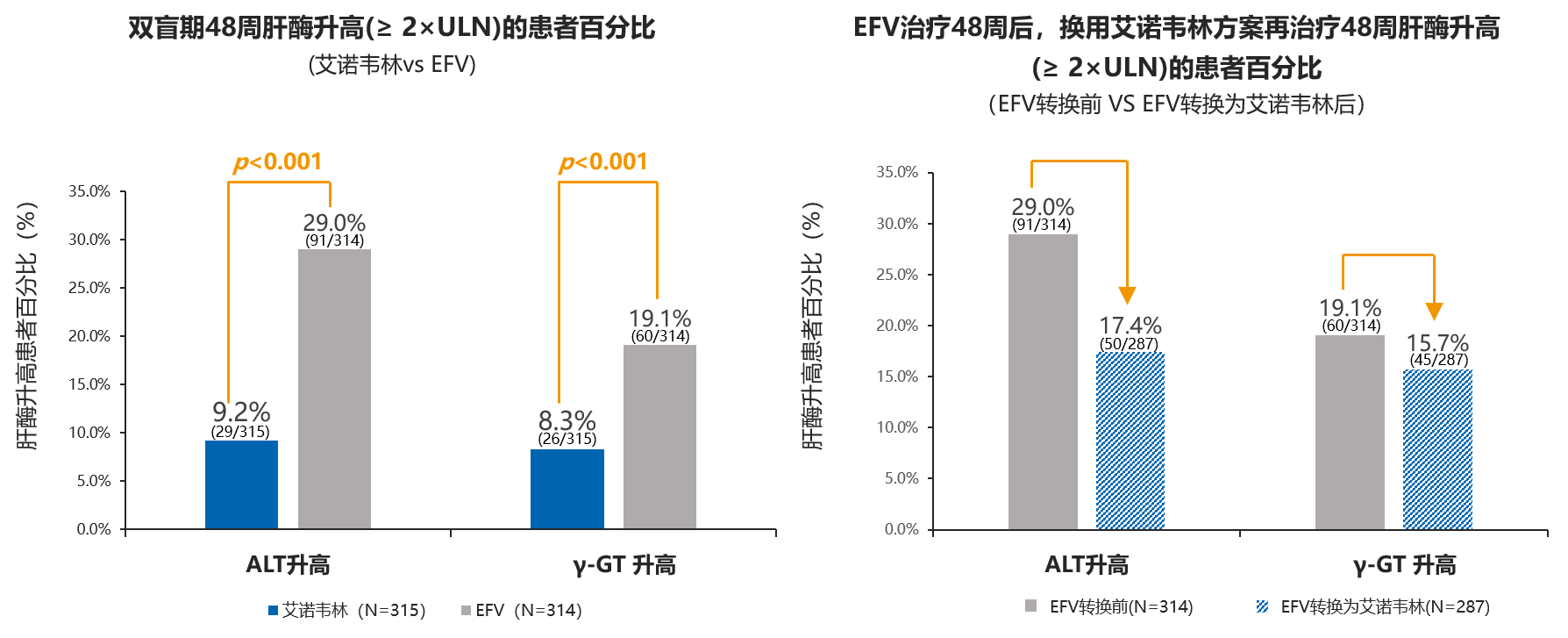
专家点评:
我国自主研发的1类艾滋病抗病毒治疗口服新药艾诺韦林首次登上国际临床医学顶级刊物,“中国循证 全球发声”。
艾诺韦林方案病毒学抑制与EFV方案相当,免疫重建更优;对血脂友好、中枢神经系统不良反应发生率及肝损等发生率低于EFV组。
EFV方案平稳转换为艾诺韦林后可继续获得病毒学抑制和免疫重建;患者血脂异常发生率、中枢神经系统不良反应发生率及肝损等发生率降低。
2023年1月4日艾诺米替(艾诺韦林+ 3TC+ TDF)上市,与国际主流复方单片合剂用药方案接轨,提升患者生活质量,提高患者依从性。
我们相信艾诺韦林方案可以为广大医务工作者提供新的治疗选择,帮助患者拥有长期健康的身心状态,回归高品质的生活。
*本材料的目的是通过介绍有关医学和科学信息和进展,提高医学专业人士的医学知识。因此,本材料仅供医学专业人士使用。本材料并非药品广告。读者不应参考或依赖本材料的任何内容,做出购买或使用任何药品的任何决定。
参考文献:DOI:https://doi.org/10.1016/j.Lanwpc.2023.100769

